组氨酸(His)虽然在蛋白质中的丰度低至~2.2%,但是它在蛋白质功能中具有许多重要作用,包括氢键供体/受体、质子穿梭、金属结合配位、金属定向共价修饰和亲核催化。近年来,His磷酸化的研究引起越来越多科学家的关注,但是,仍然缺乏专门针对His残基的稳健修饰方法以应用于组氨酸的蛋白组学研究。
近日,北京大学深圳研究生院/省部共建肿瘤化学基因组学国家重点实验室李子刚课题组,在国际知名期刊《Chemical Science》,发表了题为“Histidine-Specific bioconjugation via visible-light-promoted thioacetal activation”的研究论文,报道了一种新型的可见光催化的His化学修饰方法及其化学蛋白组学应用。
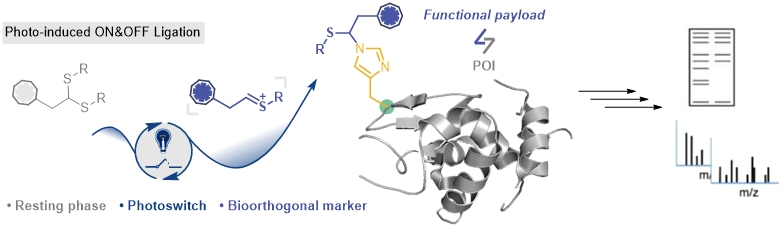
作者基于可见光对C-S键活化的新发现,开发了一种蓝光(450nm)条件下,虎红钠盐(RB)催化的“缩硫醛C-S键活化”用于标记蛋白质上His残基的方法。经过反应条件优化,该方法可以在生物兼容的可见光照射条件下,实现小分子、多肽及蛋白的高效化学修饰。通过活性蛋白质表达谱( activity-based protein profiling,ABPP)鉴定了1800种蛋白,并结合LFQ定量方法从人乳腺癌细胞系MCF7中富集了78种具有His残基的蛋白质,大多数富集的蛋白质涉及神经系统通路,与大脑中的金属积累相关。表明His残基通常存在于酶活性位点和金属结合位点,主要参与细胞代谢过程。
综上所述,本项研究报道了一个新型的可见光促进的缩硫醛C-S键活化反应用于蛋白质组氨酸残基化学修饰方法,并在乳腺癌细胞组氨酸蛋白质组研究上的应用证明了该方法的实用性,为蛋白质组氨酸残基化学修饰和蛋白组学研究的设计提供了新的思路。
北京大学深圳研究生院万川博士、王跃娜博士和深圳湾实验室坪山生物医药研发转化中心廉晨珊为该论文的共同第一作者,北京大学深圳研究生院李子刚教授、深圳湾实验室坪山生物医药研发转化中心王蕊研究员和尹丰研究员为该论文的共同通讯作者。以上工作得到了国家科技部、国家自然科学基金、广东省自然科学基金、深圳市科技创新委员会的支持。
全文链接:https://pubs.rsc.org/en/Content/ArticleLanding/2022/SC/D2SC02353A
DOI: 10.1039/D2SC02353A