酶催化反应具有高效、高选择性、条件温和、环境友好等特点,在小分子药物和活性天然产物的合成中发挥着越来越重要的作用,是合成化学和合成生物学的重要发展方向之一。与金属催化和有机小分子催化相比,天然酶催化的反应种类非常有限。因此,基于化学反应机理和蛋白质结构设计新型人工酶,有望打破酶催化与合成化学之间的壁垒,更大程度发挥酶催化的优势。针对这一问题,北京大学深圳研究生院项征课题组近期在《德国应用化学》和《美国化学会志》上发表两篇关于人工酶方面的研究论文,分别报告了以二级胺为催化基团的人工环丙烷化酶和含有机硼酸基团的人工傅克烷基化酶的研究工作。
在第一项研究中,项征课题组受到有机催化领域中手性胺催化剂可以活化羰基化合物的启发,设计合成了含D-脯氨酸侧链的非天然氨基酸DProK,并利用遗传密码子扩展技术将其选择性插入在蛋白骨架RA95.5-8的不同位点,所构建的人工酶能够通过亚胺正离子活化机制催化α,β-不饱和醛的不对称环丙烷化反应。研究者经过四轮定向进化获得了优异的突变体,有效的实现了对三个手性中心的立体控制,以高对映选择性(>99:1 e.r.)和高非对映选择性(96:4:0 d.r.)生成硝基环丙烷产物。本项研究拓展了酶的催化模式,展示了遗传密码子拓展技术在人工酶酶设计方向的潜力,为进一步拓展酶催化的非天然反应类型奠定了基础。
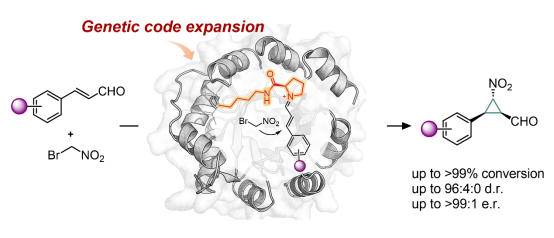
图1. 以二级胺为催化基团的人工酶设计。图片来源:Angew. Chem. Int. Ed.
在第二项研究中,项征课题组利用有机硼酸能够通过与羟基或羧基形成可逆的共价键活化底物分子的特性,通过基因密码子拓展技术在模版蛋白LmrR中引入对硼酸苯丙氨酸(pBoF)构建人工酶,用于催化不饱和酮与吲哚间的傅克烷基化反应。通过定向进化获得了催化活性和立体选择性显著提升的人工酶突变体LmrR-BAGL,并系统研究了底物的适用范围(最高>99% yield,97:3 e.r.)。研究者进一步通过全细胞催化体系实现了制备级的生物催化转化,并将这一酶促C−C键形成反应与钯催化的去芳构化反应联用,实现了一系列螺环化合物的高效高对映选择性合成。鉴于硼酸催化的多功能性,该人工酶还有望应用于催化其它各类非天然反应。
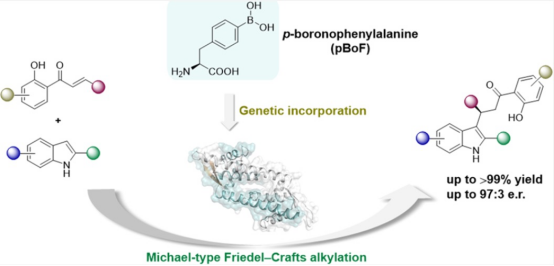
图2. 含有机硼酸基团的人工酶设计。图片来源:J. Am. Chem. Soc.
第一项研究工作发表于Angewandte Chemie International Edition,博士研究生于明珠、袁晔和南方科技大学硕士研究生李振杰为共同第一作者,为本文做出贡献的还包括项征课题组助理研究员Thittaya Kunthic和硕士研究生王鹤翔。特别感谢南方科技大学徐晨教授的指导和帮助。该工作得到了深圳市科技项目、广东省重点领域研发项目、国家自然科学基金和广东省基础与应用基础研究基金项目等基金的支持。
第二项研究工作发表于Journal of the American Chemical Society,博士研究生牟树彬、陈凯月和助理研究员Thittaya Kunthic为共同第一作者。特别感谢北京大学深圳研究生院潘峥婴特聘研究员的宝贵建议。该工作得到了深圳市科技项目、广东省重点领域研发项目等基金的支持。
References:
[1] Yu, M.-Z.#; Yuan, Y.#; Li, Z.-J.#; Kunthic, T.; Wang, H.-X.; Xu, C.; Xiang, Z*. An Artificial Enzyme for Asymmetric Nitrocyclopropanation of α,β-Unsaturated Aldehydes—Design and Evolution. Angew. Chem. Int. Ed. 2024, 63, e202401635.
[2] Mou, S.-B.#; Chen, K.-Y.#; Kunthic, T.#; Xiang, Z*. Design and Evolution of an Artificial Friedel–Crafts Alkylation Enzyme Featuring an Organoboronic Acid Residue. J. Am. Chem. Soc. 2024, ASAP.